Alterazioni del metabolismo glucidico
IN QUALI CASI VANNO RICERCATE LE CONDIZIONI DI PRE-DIABETE O DI DIABETE TIPO 2 NEL BAMBINO E NELL’ADOLESCENTE OBESO?
L’obesità pediatrica è considerata una condizione ad elevato rischio di alterazioni del metabolismo glicidico. In accordo con le linee guida dell’American Diabetes Association (ADA) (1), dell’International Society for Pediatric and Adolescent Diabetes (ISPAD)(2), della Società Italiana di Diabetologia (SID) e dell’Associazione dei Medici Diabetologi (AMD) (3) si raccomanda che nel bambino e adolescente obeso siano ricercate sia le condizioni definite come “pre-diabete” (1, 2) sia il diabete tipo 2 conclamato.
La ricerca di pre-diabete e diabete deve essere attuata nei seguenti casi:
Soggetti con BMI > 85° percentile con età > 10 anni o in pubertà + almeno due delle seguenti condizioni:
- Familiarità di primo o secondo grado per diabete tipo 2;
- Etnia a rischio (Africani o Afro-Americani, nativi Americani, Asiatici);
- Segni clinici o biochimici di insulino-resistenza o condizioni associate ad insulino-resistenza (achantosis nigricans, dislipidemia, ipertensione, sindrome dell’ovaio policistico, basso peso alla nascita);
- Storia materna di diabete gestazionale.
QUALI SONO I CRITERI PER LA DIAGNOSI DI PRE-DIABETE?
Glicemia a digiuno >100<126 mg/dl, oppure glicemia al T 120’ durante la curva da carico orale di glucosio (OGTT) >140<200 mg/dl, oppure emoglobina glicosilata (HbA1c) >6<6,5% (>42< 48 mmol/mol) (4).
QUALI SONO I CRITERI PER LA DIAGNOSI DI DIABETE?
- Glicemia casuale (random) > 200 mg/dl in presenza di sintomi (poliuria, polidipsia, astenia, perdita di peso), oppure
- Glicemia a digiuno >126 mg/dl o glicemia al T 120’ durante OGTT >200 mg/dl, o HbA1c > 6,5% (>48 mmol/L). In questi casi, in assenza di sintomi il riscontro diagnostico deve essere confermato con un secondo prelievo. Si raccomanda che l’OGTT sia effettuato dopo due giorni di dieta libera, mediante la somministrazione a digiuno di 1,75 g/kg di peso corporeo di glucosio (fino ad un massimo di 75 g) sciolto in almeno 200 ml di acqua ed assunto in 5 minuti (4).
In presenza di obesità e diabete va sempre effettuato il dosaggio degli autoanticorpi per escludere una forma auto-immunitaria.
E’UTILE IL DOSAGGIO DELL’HBA1C PER LA DIAGNOSI DI PREDIABETE E DI DIABETE ?
L’utilizzo dell'HbA1c per la diagnosi di prediabete e di diabete è ancora controverso per due motivi: a) necessità di utilizzare esclusivamente una metodica standardizzata (HPLC) allineata IFCC (International Federation of Clinical Chemistry and Laboratory Medicine) ed espressa in % oppure in mmol/L; 2) bassa concordanza fra HbA1c e OGTT (5, 6).
Tuttavia l’ADA ha confermato nel 2015 la raccomandazione di utilizzare anche l’ HbA1c in virtù della sua forte associazione longitudinale, in età pediatrica, con il diabete tipo 2, indipendentemente da glicemia a digiuno e durante carico (1, 6).
QUAL È LA PREVALENZA DELLE ALTERAZIONI DEL METABOLISMO GLICIDICO NELLA POPOLAZIONE PEDIATRICA AFFETTA DA OBESITÀ?
Le alterazioni del metabolismo glicidico sono state osservate nel 3,2-11,2%, secondo le casistiche della popolazione pediatrica italiana con obesità (7-10). La probabilità di avere intolleranza al glucosio è aumentata se l'anamnesi familiare è positiva per diabete tipo 2, se il rapporto vita/altezza è >0,6 o se la glicemia a digiuno è > 86 mg/dl (11).
QUALI SONO LE STRATEGIE TERAPEUTICHE DEL DIABETE TIPO 2?
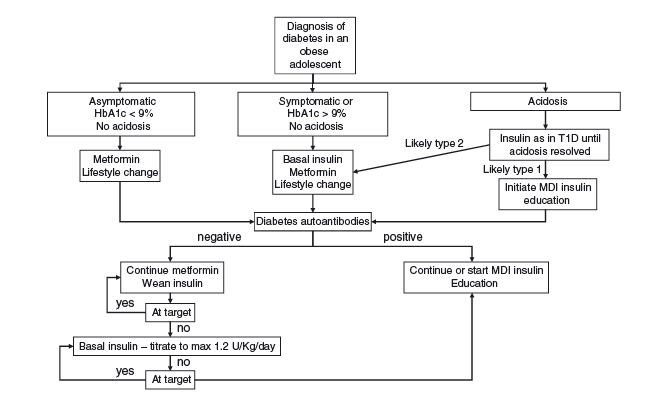
La terapia del diabete tipo 2 in età pediatrica si basa sulla modifica dello stile di vita e sull'uso di insulina e/o metformina, secondo un algoritmo basato sui livelli di compenso glicemico, da iniziare appena posta la diagnosi (2).
Algoritmo per il trattamento del diabete nell'adolescente obeso (modificato da 2)
Bibliografia
1- American Diabetes Association. Standards of Medical Care in Diabetes 2015. Diabetes Care, 2015; 38(S1): S1-S93.
2- Zeitler P, Fu J, Tandon N, Nadeau K, Urakami T, BArrett T, Maahs D, International Society for Pediatric and Adolescent Diabetes. Clinical Practice Consensus Guidelines 2014 Compendium. Type 2 diabetes in the child and adolescent. Pediatric Diabetes 2014; 15(S20): 26-46.
3- SID - AMD. Standard Italiani per la cura del Diabete Mellito 2014
4- American Diabetes Association. Diagnosis and Classification of Diabetes. Diabetes Care, 2010; 33: S62-S69.
5- Nowicka P, Santoro N, Liu H, Lartaud D, Shaw MM, Goldberg R, Guandalini C, Savoye M, Rose P, CAprio S. Utility of hemoglobin A(1c) for diagnosing prediabetes and diabetes in obese children and adolescents. Diabetes Care, 2011; 34(6):1306-11.
6- Lee JM, Eason A, Nelson C, Kazzi NG, Cowan AE, Tarini BA. Screening Practices for Identifying Type 2 Diabetes in Adolescents. J Adolesc Health, 2014; 54(2): 139-143.
7- Brufani C, Ciampalini P, Grossi A, Fiori R, Fintini D, Tozzi A, Cappa M , Barbetti F. Glucose tolerance status in 510 children and adolescents attending an obesity clinic in Central Italy. Pediatr Diabetes, 2010;11(1):47-54.
8- Cambuli VM, Incani M, Pilia S, Conugiu T, Cavallo MG, Cossu E, Sentinelli F, Mariotti S, Loche S, Baroni MG. Oral glucose tolerance test in Italian overweight/obese children and adolescents results in a very high prevalence of impaired fasting glycaemia, but not of diabetes. Diabetes Metab Res Rev, 2009; 25(6): 528-34.
9- Grandone A, Amato A, Luongo C, Santoro N, Perrone L, del Giudice EM. High-normal fasting glucose levels are associated with increased prevalence of impaired glucose tolerance in obese children. J Endocrinol Invest, 2008; 31(12): 1098-102.
10- Maffeis C, Pinelli L, Brambilla P, Banzato C, Valzolgher L, Ulmi D, Di Candia S, Cammarata B, Morandi A. Fasting plasma glucose (FPG) and the risk of impaired glucose tolerance in obese children and adolescents. Obesity (Silver Spring), 2010;18(7): 1437-42.
11- Santoro N, Amato A, Grandone A, Brienza C, Savarese P, Tartaglione N, Marzuillo P, Perrone L, Miraglia Del Giudice E. Predicting metabolic syndrome in obese children and adolescents: look, measure and ask. Obes Facts, 2013; 6(1):48-56.
